Хламидиоз — инфекционное заболевание, передающееся половым путём, вызываемое хламидиями (Chlamydia trachomatis).
| Chlamydia | ||
|---|---|---|
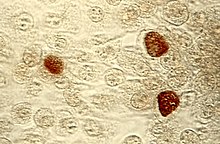
| Мазок с C. trachomatis под микроскопом | ||
| МКБ-10 | A-A, A-A | |
| МКБ-9 | , | |
| DiseasesDB | ||
| eMedicine | ||
| MeSH | ||
По статистике ежегодно хламидиозом в мире заболевает 100 млн человек, а число инфицированных хламидиями людей на всем земном шаре по самым скромным подсчётам достигает одного миллиарда. По данным ВОЗ и многочисленных отечественных и зарубежных исследователей, урогенитальный хламидиоз является одним из самых распространённых заболеваний, передаваемых половым путём, поэтому серьёзную проблему для современной венерологии представляет поиск максимально эффективных средств лечения так называемых негонококковых воспалительных заболеваний органов мочеполовой системы.
По разным данным, от 5 до 15 % молодых сексуально активных людей поражены хламидийной инфекцией. У пациентов дерматовенерологических диспансеров Российской Федерации данная инфекция встречается в 2—3 раза чаще, чем гонорея. Частота негонококковых воспалительных заболеваний органов мочеполовой системы в 5—6 раз превышает таковую у гонореи, их инкубационный период более длительный, клинические проявления менее выражены, чаще возникают осложнения, среди возбудителей преобладают хламидии. Широкое распространение хламидийной инфекции связано прежде всего с бессимптомным течением заболевания.
Содержание |
История
Хламидии способны вызывать у человека спектр органных поражений, во много раз перекрывающий таковой, например, у грамотрицательных пиогенных кокков. Действительно, редкий микроорганизм может повреждать одновременно и наружные, и внутренние половые органы, слизистую дыхательных путей, интиму сосудов и сердце, синовиальную выстилку суставов, зубы, органы зрения и слуха.Долгое время едва различимые в световой микроскоп Chlamydia trachomatis не привлекали пристального внимания медицины. Поскольку не имели ни отягощенного анамнеза, ни шумной истории открытия. Хламидии нельзя было причислить ни к вирусам, ни к бактериям. Потому что устроены и функционируют они значительно сложнее первых, но куда проще вторых.
У этого микроорганизма очень необычная история названий. Хламидии, даже задолго до зачисления их в отдельное семейство и род удостаивались пышных и необычных имён. «Миягаванеллы» (Miyagawanella), «гальпровии» (Halprowia), «бедсонии» (Bedsonia) — какими только поэтическими именами не называли этот микроорганизм.
Этиология
Chlamydia trachomatis — представляют собой неподвижные, кокковидные, грамотрицательные облигатные внутриклеточные микроорганизмы. Хламидийная инфекция поражает главным образом мочеполовую систему. В настоящее время урогенитальный хламидиоз является самой распространённой (до 60 %) причиной негонококковых уретритов. Длительное время скрыто существуя, при неблагоприятных условиях (воздействие антибиотиков, перегревание, переохлаждение, простуда) хламидии способны трансформироваться в так называемые L-формы — как бы «впадают в спячку». Данный феномен способствует длительному внутриклеточному паразитированию без конфликтов с иммунной системой хозяина. При делении клеток организма спящие хламидии передаются дочерним клеткам. Только в период иммуносупрессии (подавления защитных сил) возможно активное размножение и так называемая реверсия (пробуждение) хламидий из L-форм.У Chlamydia trachomatis разделяют следующие антигенные серотипы:
- A,B,Ba,C — вызывают трахому;
- D,E,F,G,H,I.J,K — вызывают конъюнктивит и урогенитальные инфекции;
- L1,L2,L3 — вызывают венерическую лимфогранулему.
- Chlamydia suis (от лат. род. Sus) — впервые была выделена у свиньи (Sus scrofa). Различные штаммы C. suis вызывают конъюнктивит, энтерит и пневмонию у животных и характеризуются повышенной резистентностью к сульфадиазину и тетрациклину.
- Chlamydia muridarum (от лат. сем. Muridae) — ранее рассматриваемый как третий биовар C. trachomatis (MoPn mouse pneumonitis), является возбудителем заболеваний грызунов семейства Muridae.
- В соответствии с измененной классификацией виды Chlamydia pneumoniae, Chlamydia psittaci и Chlamydia pecorum выделены в отдельный род Chlamydophila [1].
Пути заражения
Заражение хламидиозами обычно происходит половым путём, однако передача происходит не во всех случаях: если гонореей от больного партнёра заразятся во время полового контакта 3 из 4 человек, то хламидиозом — 1 из 4. Женщины более восприимчивы к хламидиозу.Инкубационный период — от 2-х недель до 1 месяца. Основной путь заражения — вагинальный, или анальный половой контакт. Дети могут инфицироваться при прохождении плода через родовые пути матери, больной хламидиозом. Также возможен контактно-бытовой путь передачи с загрязненных рук на глаза (установлено сохранение инфекционности хламидий на бытовых предметах, в том числе на хлопчатобумажных тканях, до 2-х суток при температуре 18-19 градусов).
Патогенез
- Внутриклеточное паразитирование — объединяет хламидии с вирусами, при этом хламидии не способны синтезировать АТФ и полностью зависят от энергетических ресурсов клетки — то есть в процессе паразитирования разрушают её полностью.
- Наличие клеточной оболочки — объединяет хламидии с бактериями — это позволяет применять антибиотики для лечения хламидиоза.
- Тропизм к эпителию определённых органов (мочеполовые органы, конъюнктива).
- Наличие уникального жизненного цикла.
Хламидии существуют в организме в двух формах:
- Элементарные тельца (ЭТ) — или внеклеточные инфекционные тельца.
- Ретикулярные тельца (РТ) — внутриклеточная форма возбудителя.
Первая ступень инфекционного процесса — прикрепление метаболически неактивного, но инфекционного элементарного тельца к клетке хозяина. Обычно это не реснитчатый цилиндрический или кубический эпителий (конъюнктива, уретра, эндоцервикс, эндометрий, маточные трубы).
После прикрепления следует фагоцитоз элементарного тельца, им же и индуцируемый. Внутри клетки элементарные тельца существуют в цитоплазматической вакуоли — фагосоме, где хламидии остаются весь цикл роста, а поверхностные антигены микроба ингибируют распад и лизис фагосомы. Возможно, это одна из причин хронизации инфекции. Далее элементарное тельце преобразуется в ретикулярное тельце, уже метаболически активное и способное к делению. Ретикулярное тельце неинфекционно и не может выжить вне клетки. Ретикулярные тельца делятся 8—24 часа, конденсируются и превращаются в новые элементарные тельца. Через 48—72 часа клетка разрушается и элементарные тельца выделяются во внешнюю среду. Этим начинается новый цикл размножения хламидии, который длится около 48 часов.
Хламидия напоминает вирус тем, что является полностью внутриклеточной бактерией: зависит от питательных веществ и энергии клетки — хозяина, не синтезирует АТФ, являясь энергетическим паразитом. Но, как и все бактерии, содержит как ДНК, так и РНК, размножается делением, имеет твердую оболочку наподобие грамотрицательных бактерий, которая содержит сходный липополисахарид.
Клинические проявления
Хламидиоз очень часто протекает бессимптомно, либо с минимальными проявлениями. Абсолютно без симптомов хламидиоз протекает у 46 % мужчин и 67 % женщин. Если же симптомы присутствуют, то выражены они не ярко.- Симптомы хламидиоза у женщин:
- Симптомы хламидиоза у мужчин:
В ряде случаев происходит длительное сохранение хламидий в организме в виде изолированных микроколоний на слизистых — так называемое носительство. При клиническом, инструментальном и лабораторном обследовании никаких признаков поражения органов не выявляется — то есть человек клинически здоров, и лишь при применении высокоточных методов лабораторной диагностик (ПЦР,культуральное исследование) выявляются хламидии. Это состояние связано с подавлением размножения хламидий иммунной системой организма.
Осложнения
- Болезнь Рейтера (уретро-окуло-синовиальный синдром) — характеризуется триадой симптомов: уретрит, конъюнктивит и артрит. Также при синдроме встречается различного вида поражение кожных покровов и цирцинарный баланопостит.
- Стриктура уретры — сужение мочеиспускательного канала вследствие рубцовых изменений слизистой уретры, единственным методом лечения которой является оперативное вмешательство.
- Орхоэпидидимит, ведущий к сужению выносящих спермовыводящих путей и гибели клеток Лейдига, что ведет к прекращению спермагенеза (производства сперматозоидов) и мужскому бесплодию.
- Хронический простатит, ведущий к гибели железистой ткани предстательной железы, сужению протоков простаты, изменению количества и качества секрета простаты, что приводит к обездвиживанию и быстрой гибели сперматозоидов.
- Воспалительные заболевания органов малого таза (ВЗОМТ) у женщин — хламидийная инфекция может проникнуть в матку, придатки матки, маточные трубы женщины вызывая там воспалительный процесс — эндометрит, сальпингооофорит, сальпингит. Отличительной чертой хламидиоза является образование рубцов и спаек в маточных трубах, что является причиной внематочной беременности и трубного бесплодия.
- Офтальмохламидиоз (20 %) — конъюнктивит с включениями.
- Хламидийная пневмония новорождённых (20-25 %).
- Генерализованный хламидиоз с поражением лёгких, сердца, печени, желудочно-кишечного тракта.
- Энцефалопатия с судорогами, апноэ.
- Хламидийная пневмония новорождённых — инфицирование новорождённого хламидиями во время родов от больной матери часто приводит к возникновению у них воспаления лёгких (пневмонии) с крайне тяжелым течением и с высокой летальностью.
- Синдром Фитца-Хью — Куртиса (англ.) — его считают ранним осложнением хламидийной инфекции. Проявляется как острый перитонит и перигепатит, сопровождающийся асцитом и может протекать без проявления ВЗОМТ[1][неавторитетный источник?].
Диагностика
Диагностика хламидиоза сложна, поскольку Chlamydia trachomatis — внутриклеточный паразит. В связи с этим для диагностики хламидиоза берут не мазок (слизь и выделения), а соскоб (клетки больного органа), но применение неинвазивных тестов иногда более приемлемо для пациентов. Материалом для анализа на хламидии также может стать кровь, моча и сперма у мужчин.Для выявления хламидий используются следующие лабораторные методики:
- Мини-тест.
- Микроскопический анализ (общий мазок).
- Реакция иммунофлюоресценции (РИФ).
- Иммуноферментный анализ (ИФА).
- Полимеразная цепная реакция (ПЦР).
- Посев на хламидии (культуральный метод) с определением чувствительности к антибиотикам.
Лечение
В России диагноз «хламидиоз» ставится с начала 1990-х; ранее не было ни надёжных средств диагностики данного заболевания, ни эффективных методов его лечения.В 1990-х схема лечения хламидиоза была длительной (2-3 месяца и более), сложной и многоступенчатой (последовательный приём нескольких антибиотиков, а также местные противомикробные и противогрибковые средства, гепатопротекторы и т. д.), имела ряд побочных эффектов и не всегда давала устойчивое выздоровление. Ситуация кардинально изменилась в 2000-х с появлением новых эффективных и безопасных антибиотиков: ныне курс лечения хламидиоза занимает 2-3 недели.
Поскольку Chlamydia trachomatis — внутриклеточный паразит, выбор препаратов ограничивается теми, которые способны проникать внутрь клетки. К макролидам относятся антибиотики, содержащие в молекуле макроциклическое лактановое кольцо, связанное с одним или несколькими углеродными остатками. Различия в химической структуре макролидов не столь существенны, но их физико-химические и биологические качества различаются. 14-членные макролиды — эритромицин, олеандомицин, кларитромицин, рокситромицин; 15- членный — азитромицин; 16-членные — джозамицин и спирамицин. Макролиды «нового поколения» незначительно отличаются от эритромицина по спектру действия, но имеют неполную перекрестную устойчивость с ним, улучшенную фармакокинетику и повышенный профиль безопасности.
Препаратом выбора в лечении урогенитального хламидиоза по последним международным стандартам (рекомендации ВОЗ, Европейские рекомендации 2010 г. — European guideline for the management of Chlamydia trachomatis infections) является азитромицин — однократный прием соответствующей дозы; либо применяется 7-дневный курс доксициклина. Альтернативными являются прочие макролиды, фторхинолоны. Профиль безопасности позволяет применять азитромицин при лечении беременных (категория В по FDA). Для прочих макролидов недостаточно доказательных данных (С-категория, либо не установлен уровень безопасности по FDA), чтобы можно было их рекомендовать при беременности.
Помимо антибиотика, схема лечения хламидиоза иногда включает противогрибковые препараты (флюконазол), иммуномодуляторы (интерферон); при наличии обильных выделений из уретры используют также местные противомикробные препараты).
Обязательному обследованию и, при необходимости, лечению, подлежат все партнёры, находившиеся в половом контакте с больным. В период лечения и диспансерного наблюдения половая жизнь не рекомендуется, либо используется презерватив. Во время лечения запрещён приём алкогольных напитков; рекомендуется также ограничить употребление молочных продуктов.
Контроль излеченности
Установление клинико-микробиологических критериев излеченности хламидийной инфекции проводится:- ИФА на IgA через 1.5—2 месяца после лечения (выздоровление: IgA нет).
- ИФА на IgG через 1.5—2 месяца после лечения (выздоровление: снижение титра в 4-8 раз). Однако после выздоровления титр IgG может остаться на прежнем уровне (так называемый «серологический рубец»). Поэтому большинство стандартов не рекомендуют использовать определение антител для установления излеченности хламидиоза.
- ПЦР через 1.5—2 месяца после лечения (выздоровление: ПЦР отр).

Смертність від хламідіозу у світі за країнами (Чоловік на 100 000 населення, 2004 рік)[1]
нема даних
≤10
10-20
20-30
30-40
40-50
50-60
60-70
70-80
80-90
90-100
100-110
більше 110
Хламідіоз або Урогенітальний хламідіоз — поширене інфекційне захворювання, яке відноситься до сексуально-трансмісивних хвороб. Часто спостерігається у чоловіків (не гонорейний уретрит, епідидиміт, орхіепідидиміт, проктит та ін.), жінок (кольпіт, цервіцит, ерозії, уретрит, сальпінгіт тощо) і навіть у новонароджених (зараження відбувається під час пологів). Хламідіоз на сьогодні є одним з найпоширеніших захворювань, що передаються статевим шляхом. Найчастіше вражаються органи сечостатевої системи, рідше очі і суглоби.
Зміст |
Причини
Як вказано вище, захворювання викликається хламідіями – грамнегативні бактерії, які паразитують усередині клітин епітелію, що вистилає сечостатевий тракт. Інфекція передається практично тільки статевим шляхом. Джерелом є хвора людина. Інкубаційний період становить від 7 до 30 днів.Розвиток
Запальний процес розвивається після потрапляння хламідій на чутливий до них циліндричний епітелій (у чоловіків — слизова уретри і прямої кишки, у жінок — слизова цервікального каналу, уретри і прямої кишки). Надалі процес може перейти на навколишні органи, викликаючи в них відповідну патологію. У хворих урогенітальними хламідіозами і їхніх статевих партнерів нерідко спостерігаються супутні запальні процеси іншої локалізації, що виникають при перенесенні збудника з сечостатевих органів на інші слизові: у очі, носоглотку, пряму кишку.У чоловіків, крім запалення в сечовипускному каналі, хламідії є однією з основних причин запалення яєчка, частою причиною простатиту, безпліддя, хронічного запалення суглобів (хвороба Рейтера).
У жінок хламідії можуть викликати запальні захворювання органів малого тазу (ендометрит, сальпінгіт, сальпінгоофорит), бути причиною позаматкової вагітності, викиднів, хронічного болю, безпліддя.
У новонароджених, що народжені інфікованими жінками, часто розвивається хламідійне запалення очей і легенів.
Прояви
Діапазон клінічних проявів урогенітальної хламідійной інфекції достатньо широкий: від виражених запальних явищ до відсутності якої-небудь симптоматики.Клінічні прояви урогенітального хламідіоза у чоловіків і у жінок мають свої особливості через відмінності в локалізації первинних осередків ураження (сечовипускальний канал у чоловіків, цервикальний канал у жінок). Найбільш раннім клінічним проявом урогенітального хламідіоза у чоловіків є запалення сечовипускального каналу. Початок клінічних проявів варіює від явної запальної реакції, що супроводжується рясними виділеннями з сечовипускального каналу (гостра течія) до мізерних, ледве помітних слизистих виділень без характерних ознак запалення (підгострий або торпідний перебіг). У останньому випадку хворі часто не звертаються по медичну допомогу, що веде до хронізації процесу і розвитку ускладнень. Окрім виділень хворих може турбувати свербіння у області сечовипускального каналу, незначні різі при сечовипусканні.
У жінок інфекція, як правило, протікає з мінімальними проявами, а деколи і зовсім безсимптомно. Спочатку розвивається запалення сечовипускального і/або цервикального каналу. Хворих може турбувати свербіння в сечовипускальному каналі, біль при сечовипусканні, іноді прискорені позиви на сечовипускання. Проявами запалення цервикального каналу можуть бути відчуття вологості в статевих органах, відчуття тяжкості з невеликими болями, незначні виділення з піхви. Проте, найчастіше запалення розвивається без клінічних проявів, жінки не звертаються по медичну допомогу, що приводить до розвитку важких ускладнень. Часто саме клінічні прояви ускладнень хламідійной інфекції (запалення маткових труб, яєчників, безпліддя) примушують жінок звертатися до лікаря.
Діагностика
Діагностика ґрунтується на даних анамнезу (тривало хворіють обидва партнери, безплідність). Остаточний діагноз встановлюють при виявленні хламідій у зіскребку з каналу шийки матки, піхви, уретри. Найточнішими є імуноферментні та імунофлюоресцентні методи.Лікування
При підозрі на хламідійну інфекцію або розвиток запальних захворювань сечостатевих органів і безпліддя необхідно звернутися до фахівця для обстеження і лікування. При виявленні хламідійной інфекції необхідне обов'язкове обстеження і лікування всіх осіб, що мали з хворим статеві контакти, незалежно від наявності у них клінічних проявів. На час лікування забороняють статеве життя, вживання алкогольних напоїв, гострої їжі, тривалі фізичні і психічні перевантаження. Для лікування використовують антибіотики з групи тетрацикліну, макролідів ( клацид, еритроміцин) , фторхинолонів. Іноді потрібно декілька курсів антибіотикотерапії. При необхідності, особливо при тривало протікаючій інфекції, проводять імунотерапію. Окрім цього, при розвитку ускладнень проводять симптоматичне їх лікування.Трудність лікування хламідіозу дуже часто пов'язана з одночасним невиявленим та невилікуваним трихомоніазом, збудник якого значно більший розмірами, захоплює хламідії всередину, чим унеможливлює дії на них антибіотиків. Щоб вилікувати хламідіоз з одночасно наявним трихомоніазом, необхідно спершу виявити та вилікувати трихомоніаз, лікування якого внаслідок стійкості до препаратів також може бути тривалим. Діагностування трихомоніазу часто дуже утруднене на фоні мертвих клітин епітелію.
Профілактика
Використання при статевих контактах презервативів. Широке обстеження на хламідії: обов'язковому обстеженню підлягають жінки при перериванні вагітності і при пологах, а також пари, що звертаються з приводу безпліддя.Хламидиозата (от гръцки: χλαμύδα — „наметало“) е една от най-разпространените болести, предавани по полов път.[1] Причинява се от бактерията Chlamydia trachomatis (или други видове от семейство Chlamydiaceae). Често заразените нямат симптоми. Ако инфекцията не се лекува, може да доведе до безплодие и други здравословни проблеми. Лекува се с антибиотици.
Инфекция от същата бактерия в очите води до болестното състояние трахома и е една от водещите причини за ослепяване и лошо зрение в света.[2][3]
Бележки
- ↑ Тест с урина открива хламидия за час. // trud.bg. 31.07.09.
- ↑ Thylefors B, Négrel AD, Pararajasegaram R, Dadzie KY. Global data on blindness. // Bulletin of the World Health Organization 73 (1). 1995. с. 115–21.
- ↑ Resnikoff S, Pascolini D, Etya'ale D et al.. Global data on visual impairment in the year 2002. // Bulletin of the World Health Organization 82 (11). 2004. с. 844–851.
For chlamydia's life cycle, see Chlamydia (genus). For infectious agents previous designated Chlamydiae, see Chlamydophila.
| Chlamydia | |
|---|---|
| Classification and external resources | |
 Pap smear showing C. trachomatis (H&E stain) |
|
| ICD-10 | A55-A56.8, A70-A74.9 |
| ICD-9 | 099.41, 483.1 |
| DiseasesDB | 2384 |
| eMedicine | med/340 |
| MeSH | D002690 |
C. trachomatis is naturally found living only inside human cells. Chlamydia can be transmitted during vaginal, anal, or oral sex, and can be passed from an infected mother to her baby during vaginal childbirth. Between half and three-quarters of all women who have a chlamydia infection of the cervix (cervicitis) have no symptoms and do not know that they are infected. In men, infection of the urethra (urethritis) is usually symptomatic, causing a white discharge from the penis with or without pain on urinating (dysuria). Occasionally, the condition spreads to the upper genital tract in women (causing pelvic inflammatory disease) or to the epididymis in men (causing epididymitis). If untreated, chlamydial infections can cause serious reproductive and other health problems with both short-term and long-term consequences.
Chlamydia conjunctivitis or trachoma is a common cause of blindness worldwide. The World Health Organization (WHO) estimates that it accounted for 15% of blindness cases in 1995, but only 3.6% in 2002.[3][4][5]
Contents |
Signs and symptoms
Genital disease

Chlamydial cervicitis in a female patient characterized by mucopurulent cervical discharge, erythema, and inflammation.

Male patients may develop a white, cloudy or watery discharge (shown) from the tip of the penis.
Women
Chlamydial infection of the neck of the womb (cervicitis) is a sexually transmitted infection which is asymptomatic for about 50-70% of women infected with the disease. The infection can be passed through vaginal, anal, or oral sex. Of those who have an asymptomatic infection that is not detected by their doctor, approximately half will develop pelvic inflammatory disease (PID), a generic term for infection of the uterus, fallopian tubes, and/or ovaries. PID can cause scarring inside the reproductive organs, which can later cause serious complications, including chronic pelvic pain, difficulty becoming pregnant, ectopic (tubal) pregnancy, and other dangerous complications of pregnancy.Chlamydia is known as the "Silent Epidemic" because in women, it may not cause any symptoms in 75% of cases,[6] and can linger for months or years before being discovered. Symptoms that may occur include unusual vaginal bleeding or discharge, pain in the abdomen, painful sexual intercourse (dyspareunia), fever, painful urination or the urge to urinate more frequently than usual (urinary urgency).
Men
In men, chlamydia shows symptoms of infectious urethritis (inflammation of the urethra) in about 50% of cases.[6] Symptoms that may occur include: a painful or burning sensation when urinating, an unusual discharge from the penis, swollen or tender testicles, or fever. Discharge, or the purulent exudate, is generally less viscous and lighter in color than for gonorrhea. If left untreated, it is possible for chlamydia in men to spread to the testicles causing epididymitis, which in rare cases can cause sterility if not treated within 6 to 8 weeks. Chlamydia is also a potential cause of prostatitis in men, although the exact relevance in prostatitis is difficult to ascertain due to possible contamination from urethritis.[7]Eye disease
Main article: Trachoma
Chlamydia conjunctivitis or trachoma was once the most important
cause of blindness worldwide, but its role diminished from 15% of
blindness cases by trachoma in 1995 to 3.6% in 2002.[3][4] The infection can be spread from eye to eye by fingers, shared towels or cloths, coughing and sneezing and eye-seeking flies.[8] Newborns can also develop chlamydia eye infection through childbirth (see below). Using the SAFE strategy (acronym for surgery for in-growing or in-turned lashes, antibiotics, facial cleanliness, and environmental improvements), the World Health Organisation aims for the global elimination of trachoma by 2020 (GET 2020 initiative).[9][10]Rheumatological conditions
Chlamydia may also cause reactive arthritis (reiter's syndrome) - the triad of arthritis, conjunctivitis and urethritis (inflammation of the urethra) - especially in young men. About 15,000 men develop reactive arthritis due to chlamydia infection each year in the U.S., and about 5,000 are permanently affected by it. It can occur in both sexes, though is more common in men.Perinatal infections
As many as half of all infants born to mothers with chlamydia will be born with the disease. Chlamydia can affect infants by causing spontaneous abortion; premature birth; conjunctivitis, which may lead to blindness; and pneumonia. Conjunctivitis due to chlamydia typically occurs one week after birth (compared with chemical causes (within hours) or gonorrhea (2–5 days)).Other conditions
Chlamydia trachomatis is also the cause of lymphogranuloma venereum, an infection of the lymph nodes and lymphatics. It usually presents with genital ulceration and swollen lymph nodes in the groin, but it may also manifest as proctitis (inflammation of the rectum), fever or swollen lymph nodes in other regions of the body.[11]Transmission
Chlamydia can be transmitted during vaginal, anal, or oral sex. Chlamydia can also be passed from an infected mother to her baby during vaginal childbirth.[12]Pathophysiology
Chlamydiae have the ability to establish long-term associations with host cells. When an infected host cell is starved for various nutrients such as amino acids (for example, tryptophan),[13] iron, or vitamins, this has a negative consequence for Chlamydiae since the organism is dependent on the host cell for these nutrients. Long-term cohort studies indicate that approximately 50% of those infected clear within a year, 80% within two years, and 90% within three years.[14]The starved chlamydiae enter a persistent growth state wherein they stop cell division and become morphologically aberrant by increasing in size.[15] Persistent organisms remain viable as they are capable of returning to a normal growth state once conditions in the host cell improve.
There is much debate as to whether persistence has in vivo relevance. Many believe that persistent chlamydiae are the cause of chronic chlamydial diseases. Some antibiotics such as β-lactams can also induce a persistent-like growth state, which can contribute to the chronicity of chlamydial diseases.
Screening
For sexually active women who are not pregnant, screening is recommended in those under 25 and others at risk of infection.[16] Risk factors include a history of chlamydial or other sexually transmitted infection, new or multiple sexual partners, and inconsistent condom use.[17] For pregnant women, guidelines vary: screening women with age or other risk factors is recommended by the U.S. Preventive Services Task Force (USPSTF) (which recommends screening women under 25) and the American Academy of Family Physicians (which recommends screening women aged 25 or younger). The American College of Obstetricians and Gynecologists recommends screening all at risk, while the Centers for Disease Control and Prevention recommend universal screening of pregnant women.[16] The USPSTF acknowledges that in some communities there may be other risk factors for infection, such as ethnicity.[16] Evidence-based recommendations for screening initiation, intervals and termination are currently not possible.[16] There is no universal agreement on screening men for chlamydia.[why?]In England and Wales the NHS National Chlamydia Screening Programme (NCSP) aims to
- Prevent and control chlamydia infection through early detection and treatment of asymptomatic infection;
- Reduce onward transmission to sexual partners;
- Prevent the consequences of untreated infection;
- Test at least 25 percent of the sexually active under 25 population annually.[18]
Diagnosis
The diagnosis of genital chlamydial infections evolved rapidly from the 1990s through 2006. Nucleic acid amplification tests (NAAT), such as polymerase chain reaction (PCR), transcription mediated amplification (TMA), and the DNA strand displacement amplification (SDA) now are the mainstays. NAAT for chlamydia may be performed on swab specimens collected from the cervix (women) or urethra (men), on self-collected vaginal swabs, or on voided urine.[19] Urine and self-collected swab testing facilitates the performance of screening tests in settings where genital examination is impractical. At present, the NAATs have regulatory approval only for testing urogenital specimens, although rapidly evolving research indicates that they may give reliable results on rectal specimens.Because of improved test accuracy, ease of specimen management, convenience in specimen management, and ease of screening sexually active men and women, the NAATs have largely replaced culture, the historic gold standard for chlamydia diagnosis, and the non-amplified probe tests. The latter test is relatively insensitive, successfully detecting only 60-80% of infections in asymptomatic women, and often giving falsely positive results. Culture remains useful in selected circumstances and is currently the only assay approved for testing non-genital specimens.
Treatment
C. trachomatis infection can be effectively cured with antibiotics once it is detected. Current guidelines recommend azithromycin, doxycycline, erythromycin, or ofloxacin.[20] Agents recommended for pregnant women include erythromycin or amoxicillin.[21]An option for treating partners of patients (index cases) diagnosed with chlamydia or gonorrhea is patient-delivered partner therapy (PDT or PDPT), which is the clinical practice of treating the sex partners of index cases by providing prescriptions or medications to the patient to take to his/her partner without the health care provider first examining the partner.[22]
Epidemiology

Age-standardized death from chlamydia per 100,000 inhabitants in 2004.[23]
no data
≤10
10-20
20-30
30-40
40-50
50-60
60-70
70-80
80-90
90-100
100-110
more than 110
Chlamydia causes more than 250,000 cases of epididymitis in the U.S. each year. Chlamydia causes 250,000 to 500,000 cases of PID every year in the United States. Women infected with chlamydia are up to five times more likely to become infected with HIV, if exposed.[26]
Evolution
Recent phylogenetic studies have revealed that Chlamydia likely shares a common ancestor with cyanobacteria, the group containing the endosymbiont ancestor to the chloroplasts of modern plants, hence, Chlamydia retains unusual plant-like traits, both genetically and physiologically. In particular, the enzyme L,L-diaminopimelate aminotransferase, which is related to lysine production in plants, is also linked with the construction of chlamydia's cell wall. The genetic encoding for the enzymes is remarkably similar in plants, cyanobacteria, and Chlamydia, demonstrating a close common ancestry.[27] This unexpected discovery may help scientists develop new treatment avenues: if scientists could find a safe and effective inhibitor of L,L-diaminopimelate aminotransferase, they might have a highly effective and extremely specific new antibiotic against chlamydia.[citation needed]References
- ^ "www.chlamydiae.com (professional) - Taxonomy diagram". Retrieved 2007-10-27.
- ^ Chlamydia fact sheet from the Centers for Disease Control and Prevention
- ^ a b Thylefors B, Négrel AD, Pararajasegaram R, Dadzie KY (1995). "Global data on blindness". Bull World Health Organ 73 (1): 115–21. PMC 2486591. PMID 7704921.
- ^ a b Resnikoff S, Pascolini D, Etya'ale D et al. (2004). "Global data on visual impairment in the year 2002". Bull World Health Organ 82 (11): 844–851. PMC 2623053. PMID 15640920.
- ^ Belland R, Ojcius D, Byrne G (2004). "Chlamydia". Nat Rev Microbiol 2 (7): 530–1. doi:10.1038/nrmicro931. PMID 15248311.
- ^ a b "FreeTest.Me - About Chlamydia". Retrieved 2008-12-15.
- ^ Wagenlehner FM, Naber KG, Weidner W (2006). "Chlamydial infections and prostatitis in men". BJU Int. 97 (4): 687–90. doi:10.1111/j.1464-410X.2006.06007.x. PMID 16536754.
- ^ Mabey DC, Solomon AW, Foster A (2003). "Trachoma". Lancet 362 (9379): 223–9. doi:10.1016/S0140-6736(03)13914-1. PMID 12885486.
- ^ World Health Organisation. Trachoma. Accessed March 17, 2008.
- ^ Ngondi J, Onsarigo A, Matthews F, et al. (2006). "Effect of 3 years of SAFE (surgery, antibiotics, facial cleanliness, and environmental change) strategy for trachoma control in southern Sudan: a cross-sectional study". Lancet 368 (9535): 589–95. doi:10.1016/S0140-6736(06)69202-7. PMID 16905023.
- ^ Williams D, Churchill D (2006). "Ulcerative proctitis in men who have sex with men: an emerging outbreak". BMJ 332 (7533): 99–100. doi:10.1136/bmj.332.7533.99. PMC 1326936. PMID 16410585.
- ^ http://www.cdc.gov/std/chlamydia/stdfact-chlamydia.htm
- ^ Leonhardt RM, Lee SJ, Kavathas PB, Cresswell P (2007). "Severe Tryptophan Starvation Blocks Onset of Conventional Persistence and Reduces Reactivation of Chlamydia trachomatis". Infect. Immun. 75 (11): 5105–17. doi:10.1128/IAI.00668-07. PMC 2168275. PMID 17724071.
- ^ Fairley et al., CK; Gurrin, L; Walker, J; Hocking, JS (2007). ""Doctor, How Long Has My Chlamydia Been There?" Answer:"... Years"". Sexually Transmitted Diseases 34 (9): 727–8. doi:10.1097/OLQ.0b013e31812dfb6e. PMID 17717486.
- ^ Mpiga P, Ravaoarinoro M (2006). "Chlamydia trachomatis persistence: an update". Microbiol. Res. 161 (1): 9–19. doi:10.1016/j.micres.2005.04.004. PMID 16338585.
- ^ a b c d Meyers D, Wolff T, Gregory K. et al. USPSTF Recommendations for STI Screening. Am Fam Physician. 2008;77(6):819-824.
- ^ U.S. Preventive Services Task Force (2007). "Screening for chlamydial infection: U.S. Preventive Services Task Force recommendation statement". Ann Intern Med 147 (2): 128–34. PMID 17576996.
- ^ "National Chlamydia Screening Programme Data tables". Retrieved 2009-08-28.
- ^ Gaydos CA et al (2004). Comparison of three nucleic acid amplification tests for detection of Chlamydia trachomatis in urine specimens. J Clin Microbio 42(7):3041-3045. doi:10.1128/JCM.42.7.3041-3045.2004
- ^ al.], David N. Gilbert ... [et. The Sanford guide to antimicrobial therapy 2011. Sperryville, VA: Antimicrobial Therapy, Inc.. pp. 20. ISBN 1-930808-65-8.
- ^ "Diagnosis and Treatment of Chlamydia trachomatis Infection - April 15, 2006 - American Family Physician". Retrieved 2010-10-30.
- ^ Expedited Partner Therapy in the Management of Sexually Transmitted Diseases (2 February 2006) U.S. DEPARTMENT OF HEALTH AND HUMAN SERVICES PUBLIC HEALTH SERVICE. Centers for Disease Control and Prevention National Center for HIV, STD, and TB Prevention
- ^ "WHO Disease and injury country estimates". World Health Organization. 2004. Retrieved Nov. 11, 2009.
- ^ "STD Trends in the United States: 2010 National Data for Gonorrhea, Chlamydia, and Syphilis". Centers for Disease Control and Prevention (CDC). 22 November 2010. Retrieved 25 January 2012.
- ^ "Chlamydia". UK Health Protection Agency. Retrieved 31 August 2012.
- ^ "STD Facts - Chlamydia". Retrieved 2007-10-26.
- ^ McCoy AJ, Adams NE, Hudson AO, Gilvarg C, Leustek T, Maurelli AT (2006). "L,L-diaminopimelate aminotransferase, a trans-kingdom enzyme shared by Chlamydia and plants for synthesis of diaminopimelate/lysine". Proc. Natl. Acad. Sci. U.S.A. 103 (47): 17909–14. doi:10.1073/pnas.0608643103. PMC 1693846. PMID 17093042.
External links
| Wikimedia Commons has media related to: Chlamydia |
- Chlamydia Fact Sheet from the CDC
- Links to chlamydia pictures at University of Iowa
- The National Chlamydia Screening Programme – The NCSP's official website containing information.
- Freetest.me – National free postal testing service operating across England.
| [hide] | |||||
|---|---|---|---|---|---|
| Bacterial | |||||
| Protozoal | |||||
| Parasitic | |||||
| Viral | |||||
| General inflammation |
|||||
|
| |||||
| Prostatitis | |
|---|---|
| Classification and external resources | |
 Micrograph showing an inflamed prostate gland, the histologic correlate of prostatitis. A normal non-inflamed prostatic gland is seen on the left of the image. H&E stain. |
|
| ICD-10 | N41 |
| ICD-9 | 601 |
| DiseasesDB | 10801 |
| MedlinePlus | 000524 |
| eMedicine | emerg/488 |
| MeSH | D011472 |
Contents |
Classification
The term prostatitis refers, in its strictest sense, to histological (microscopic) inflammation of the tissue of the prostate gland. Like all forms of inflammation, it can be associated with an appropriate response of the body to an infection, but it also occurs in the absence of infection.In 1999, the National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK) devised a new classification system.[2][3] For more specifics about each type of prostatitis, including information on symptoms, treatment, and prognosis, follow the links to the relevant full articles.
| Category | Pain? | Bacteria? | WBCs? | NIDDK (Current) |
Description | Meares/Stamey (Old) |
|---|---|---|---|---|---|---|
| I | yes | yes | yes | Acute prostatitis | Acute prostatitis is a bacterial infection of the prostate gland that requires urgent medical treatment. | Acute bacterial prostatitis |
| II | ± | yes | yes | Chronic bacterial prostatitis | Chronic bacterial prostatitis is a relatively rare condition that usually presents as intermittent urinary tract infections. | Chronic bacterial prostatitis |
| IIIa | yes | no | yes | Inflammatory CP/CPPS | Chronic prostatitis/chronic pelvic pain syndrome, accounting for 90%-95% of prostatitis diagnoses,[4] used to be known as chronic nonbacterial prostatitis. | Nonbacterial prostatitis |
| IIIb | yes | no | no | Noninflammatory CP/CPPS | Prostatodynia | |
| IV | no | no | yes | Asymptomatic inflammatory prostatitis | Asymptomatic inflammatory prostatitis patients have no history of genitourinary pain complaints, but leukocytosis is noted, usually during evaluation for other conditions. Between 6-19% of men have pus cells in their semen but no symptoms.[5] | (none) |
The conditions are distinguished by the different presentation of pain, white blood cells (WBCs) in the urine, duration of symptoms and bacteria cultured from the urine. To help express prostatic secretions that may contain WBCs and bacteria, prostate massage is sometimes used.[7]
See also
| Wikipedia books are collections of articles that can be downloaded or ordered in print. | |
- Interstitial cystitis — a related disease.
- Granulomatous prostatitis.
References
- ^ Collins MM, Stafford RS, O'Leary MP, Barry MJ (1998). "How common is prostatitis? A national survey of physician visits". J. Urol. 159 (4): 1224–8. doi:10.1016/S0022-5347(01)63564-X. PMID 9507840.
- ^ Krieger JN, Nyberg L, Nickel JC (July 1999). "NIH consensus definition and classification of prostatitis". JAMA 282 (3): 236–7. doi:10.1001/jama.282.3.236. PMID 10422990.
- ^ J. Curtis Nickel (1999). Textbook of prostatitis. Taylor & Francis. pp. 27–. ISBN 978-1-901865-04-2. Retrieved 18 April 2010.
- ^ Habermacher GM, Chason JT, Schaeffer AJ (2006). "Prostatitis/chronic pelvic pain syndrome". Annu. Rev. Med. 57: 195–206. doi:10.1146/annurev.med.57.011205.135654. PMID 16409145.
- ^ Korrovits P, Ausmees K, Mändar R, Punab M (June 2008). "Prevalence of asymptomatic inflammatory (National Institutes of Health Category IV) prostatitis in young men according to semen analysis". Urology 71 (6): 1010–5. doi:10.1016/j.urology.2007.12.082. PMID 18455767.
- ^ Meares EM, Stamey TA (March 1968). "Bacteriologic localization patterns in bacterial prostatitis and urethritis". Invest Urol 5 (5): 492–518. PMID 4870505.
- ^ "Prostatitis: Benign Prostate Disease: Merck Manual Professional". Retrieved 2011-07-11.
External links
|
||



Лучшие противовоспалительные средства от простатита http://prostodin.today/
ОтветитьУдалить